Фирма «Технолуч» выпускает несколько видов Самоочищающегося стекла с
покрытиями TiO2. Метод нанесения покрытий – реактивное распыление в вакууме.
Метод является экологически безопасным, поскольку все процессы
происходят в вакуумной камере и не сопровождаются образованием каких
либо вредных отходов.
Технические характеристики стекла с применением ТiО2-покрытия
где,
• К уф % - пропускание в ультрафиолетовом диапазоне спектра;
• К пр % - пропускание в видимом диапазоне спектра;
• К отр % - отражение в видимом диапазоне спектра со стороны покрытия;
• К отр.ст % - отражение в видимом диапазоне спектра со стороны стекла;
• К пр.с. % - пропускание солнечной энергии в видимом и инфракрасном диапазоне излучения.
Фото объектов с применением самоочищающегося стекла
В ЧЕМ ВОЛШЕБНАЯ СИЛА TiO2 ПОКРЫТИЯ?
Диоксид титана – один из самых распространенных материалов в нашей повседневной жизни. Он широко используется в красках, косметике и пищевых продуктах. Сегодня ежегодное потребление диоксида титана в мире превышает три миллиона тонн. Специалисты считают, что потребление диоксида титана тесно связано с жизненным уровнем в стране.
Диоксид титана, который используется как пигмент в краске, отличается от диоксида титана, который используется как фотокатализатор.
Диоксид титана является полупроводником и становится химически активным только после его облучения ультрафиолетовым светом. Длительное время химическая активность диоксида титана под воздействием ультрафиолетового света была проблемой, которую необходимо было решить, когда TiO2 использовался как белый пигмент в краске, так как краска могла менять свой цвет.
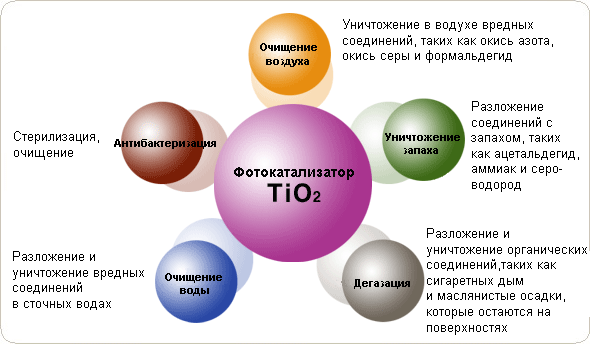 С другой стороны, диоксид титана как фотокатализатор позволяет этой активности играть положительную роль, а именно, разлагать такие материалы, как грязь, сажа, химические препараты и раздражители, токсические препараты, запах дыма сигарет, бактерии или органические материалы. По этой причине можно ожидать, что разработка фотокаталитических технологий на основе TiO2 скоро станет новой отраслью промышленности уже в этом столетии.
С другой стороны, диоксид титана как фотокатализатор позволяет этой активности играть положительную роль, а именно, разлагать такие материалы, как грязь, сажа, химические препараты и раздражители, токсические препараты, запах дыма сигарет, бактерии или органические материалы. По этой причине можно ожидать, что разработка фотокаталитических технологий на основе TiO2 скоро станет новой отраслью промышленности уже в этом столетии.
Научное изучение фотокатализа на TiO2-покрытиях началось около 30 лет назад. За это время направление научных исследований менялось несколько раз. Первоначально, фотокаталитическую способность диоксида титана пытались применить для получения водорода из воды, затем пристальное внимание привлекла способность TiO2-покрытия уничтожать вирусы и раковые клетки, разлагать органические загрязнения. В настоящее время уже более 1000 фирм, используя уникальные свойства TiO2-покрытия, создают технологии и оборудование для очистки воздуха и воды.
Например, это покрытие может защитить стекла, используемые на осветительных приборах в туннелях, от загрязнения выхлопными газами автомобильного транспорта. Грязь и сажа не задерживается на брезенте, который покрывает крышу Tokyo Dome (Токио). Здания Оперы в Сиднее (Sydney Opera House) не очищалось бы дождевой водой, если бы на крыше не было TiO2-покрытия. Используя ту же технологию, можно уберечь ветровые стекла, зеркала и очки от «запотевания» водяным паром. TiO2, как фотокатализатор, проявляют изумительные бактерицидные и дезинфицирующие свойства.
Приведенные выше примеры использования диоксида титана показывают, насколько различны функции фотокатализаторов на основе TiO2. Новшества в развитии технологии фотокатализа могут изменить восприятие людей, как о чистоте, так и об очистке окружающей среды.
Что может послужить тому причиной?
Современные методы очистки базируются на предотвращении неконтролируемого попадания отходов, прежде всего, в воздух, воду и почву.
Общепринятыми методами очистки и дезинфекции является хлорирование и озонирование, использование бактерицидных ламп, применение различных фильтров, использование высоких температур или дезинфицирующих веществ. Все эти методы имеют избирательное действие, т.е. они не в состоянии обезвредить все группы микроорганизмов или устранить химические загрязнения. И, последнее, после того как «вредные» вещества уже «пойманы» различными фильтрами необходимо решить, а куда же деть отловленную гадость.
Именно по этой причине пристальное внимание специалистов, работающих в области охраны окружающей среды, сосредоточено на поиске процессов и методов, позволяющих преобразовывать вредные вещества в безопасные компоненты, а заодно и уничтожить патологические микроорганизмы.
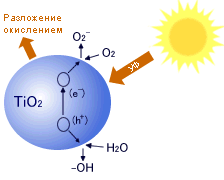 Использование фотокаталитического окисления или гетерогенного фотокатализа позволяет решать обе упомянутые задачи одновременно.
Использование фотокаталитического окисления или гетерогенного фотокатализа позволяет решать обе упомянутые задачи одновременно.
Гетерогенный фотокатализ – безопасный и высокоэффективный способ разложения веществ и микроорганизмов до абсолютно безвредных компонентов под действием света в присутствии катализатора. В качестве катализатора используются широко известные полупроводники на основе оксидов металлов (TiO2, ZnO, Fe2O3 и др.).
В большинстве случаев в качестве катализатора используется TiO2, как наиболее устойчивое, недорогое и безопасное, химически и биологически инертное соединение, обладающее наибольшей фотокаталитической активностью при освещении натуральным или искусственным светом.
Первыми процесс фотокаталитического расщепления воды для получения водорода на TiO2 электродах описали Fujishima и Honda в 1972.
В 1985 году Matsunaga с сотрудниками впервые сообщили о бактерицидной активности TiO2. С этого времени исследования в этом направлении получило широкое распространение во всем мире.
За последние годы тысячи химических соединений, большинство из которых занесены в список основных загрязняющих веществ и токсинов, вирусов и раковых клеток были тестированы на возможность их окисления в процессе гетерогенного катализа. Лучше всего изучены: углеводороды и их производные, спирты, эфиры, фенолы, альдегиды, кислоты.
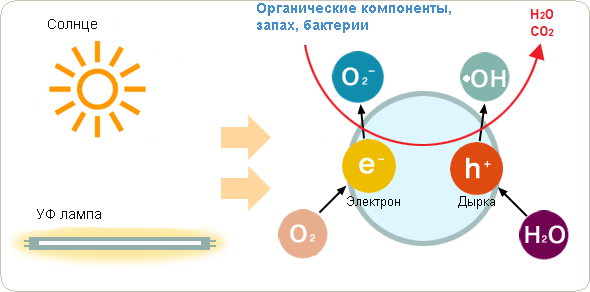 Основную роль в процессе расщепления веществ на поверхности фотокатализатора под действием света играет образование свободных носителей заряда – электронов и дырок при облучении поверхности фотокатализатора (TiO2) светом с длиной волны менее 390 нм.
Основную роль в процессе расщепления веществ на поверхности фотокатализатора под действием света играет образование свободных носителей заряда – электронов и дырок при облучении поверхности фотокатализатора (TiO2) светом с длиной волны менее 390 нм.
Процессы разложения происходят при комнатной температуре и не требуют применения опасных и дорогостоящих препаратов, а в качестве источника света могут быть использованы стандартные лампы дневного света либо натуральный солнечный свет.
Фотокаталитическое разрушение вещества применяют в случаях, когда традиционные средства очистки не помогают, в частности, при уничтожении пестицидов, отходов военных предприятий (тяжелые металлы, авиационное топливо, органические вещества, обезжиривающие агенты и другие химические побочные продукты от производства оружия) или химических красителей. Положительные результаты были достигнуты при очистке воды от экстрагенов (половые гормоны, использующиеся при производстве многих медикаментов), которые вызывают серьезные нарушения в развитии живых организмов или рост раковых заболеваний у людей.
Исследования показали, что чувствительность микроорганизмов к фотокаталитическому расщеплению уменьшается в следующем порядке:
• вирусы;
• бактерии;
• споры бактерий.
За последние годы фотокаталитические пленки TiO2 становятся все более и более привлекательными для использования в различных областях, в первую очередь, при создании дополнительных или основных фильтров для дезинфекции и очистки воды и воздуха.
Помимо бактерицидного действия TiO2 обладает также способностью к самоочищению.
В последнее время особое внимание уделяется созданию самоочищающихся и обладающих противотуманным эффектом поверхностей с покрытием из TiO2.
НА ЧЕМ ОСНОВАНЫ СВОЙСТВА ПОКРЫТИЯ К САМООЧИЩЕНИЮ?
Поверхность любых материалов обычно отталкивает воду. Степень отталкивания воды веществом можно выразить с помощью контактного угла капли воды к поверхности. На стекле или других неорганических материалах, вода имеет контактный угол, колеблющийся от 30 до 90 градусов. У пластика контактный угол обычно от 70 до 80 градусов. У водоотталкивающего пластика угол может превышать 80 градусов.
В настоящее время неизвестны вещества, на поверхности которых угол наклона капли воды был менее 10 градусов. И только пленка из диоксида титана может похвастаться такими результатами.
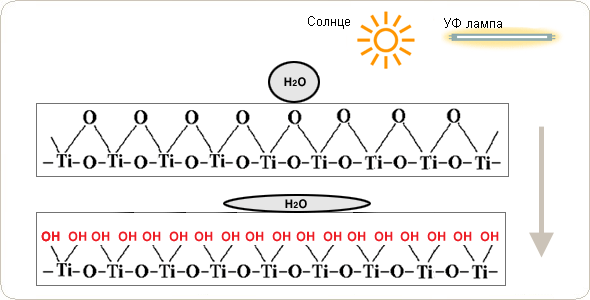
Тонкая пленка, состоящая из TiO2 фотокатализатора, в сочетании с подходящими добавками демонстрирует начальный контактный угол для воды от 30 до 80 градусов. На этой же поверхности, когда ее подвергают ультрафиолетовому облучению, капля воды меняет контактный угол. Угол постепенно уменьшается и после 4…24 часов облучения достигает почти нуля градусов. На этом этапе, поверхность из гидрофобной (боящейся воды) становится полностью гидрофильной (любящей воду) и такую поверхность называют “супергидрофильной”.
Поверхность сохраняет небольшой контактный угол для воды в течение 1-2 дней без дополнительного облучения ультрафиолетовыми лучами. Затем контактный угол медленно увеличивается, и поверхность становится снова гидрофобной. Но, «супергидрофильность» легко восстанавливается при последующем воздействии на поверхность ультрафиолетовым светом. Короче говоря, TiO2-покрытие является единственно известным практическим «супергидрофильным» материалом, который демонстрирует свои стабильные свойства.
ПРИНЦИП ДЕЙСТВИЯ ТiО2 КАК ФОТОКАТАЛИЗАТОРА
ТiО2 – полупроводниковое соединение. Согласно современным представлениям, в таких соединениях электроны могут находиться в двух состояниях – свободном и связанном. В первом состоянии электроны движутся по кристаллической решетке, образованной катионами Тi4+ и анионами кислорода O2-. Во втором состоянии – основном, электроны связаны с каким-либо ионом кристаллической решетки и участвуют в образовании химической связи. Для перевода электрона из связанного состояния в свободное состояние, необходимо затратить энергию не менее 3,2 эВ. Эта энергия может быть доставлена квантами света с длиной волны < 390 нм (ультрафиолетовое излучение). Таким образом, при поглощении света в объеме частицы ТiО2 рождаются свободный электрон и электронная вакансия (в физике полупроводников такая электронная вакансия называется дыркой).
Электрон и дырка – достаточно подвижные образования и, двигаясь в частице полупроводника, часть из них рекомбинирует (возвращается в связанное состояние), а часть выходит на поверхность и захватывается ею.
Захваченные на поверхности электрон и дырка, являются вполне конкретными химическими частицами. Химически они чрезвычайно активны.
 В терминах окислительно-восстановительных потенциалов реакционная способность электрона и дырки на поверхности ТiО2 характеризуется следующими величинами: потенциал электрона -0,1 В, потенциал дырки ~ +3 В относительно нормального водородного электрода. Иными словами, электрон способен реагировать с кислородом, рождая мощные окислительные радикалы O- и ОН.
В терминах окислительно-восстановительных потенциалов реакционная способность электрона и дырки на поверхности ТiО2 характеризуется следующими величинами: потенциал электрона -0,1 В, потенциал дырки ~ +3 В относительно нормального водородного электрода. Иными словами, электрон способен реагировать с кислородом, рождая мощные окислительные радикалы O- и ОН.
Дырка реагирует либо с водой, либо с любым адсорбированным органическим (в ряде случаев и неорганическим) соединением.
ОН- или О- радикалы также способны окислить любое органическое соединение. И таким образом, поверхность ТiО2 под светом становится сильнейшим окислителем.
Последовательность реакций в пленке ТiО2 проходит несколько стадий:
• поглощение света – рождение электрон - дырочных пар;
• диффузия электронов и дырок к поверхности полупроводника;
• объемная рекомбинация электронов и дырок;
• поверхностная рекомбинация электронов и дырок;
• полезные реакции электронов и дырок с адсорбированными молекулами.
К сожалению, к настоящему моменту нет надежных объяснений, связывающих активность ТiО2-покрытия с его свойствами. Из практики известно, что наибольшей фотокаталитической активностью обладают образцы ТiО2 с кристаллической модификацией анатаза и не содержащие большого числа примесей. Поэтому изготовление активного ТiО2-покрытия – предмет опыта каждой компании. Тем не менее, практически все, кто занимается прикладным фотокатализом, обладают оригинальными методиками синтеза высокоактивного ТiО2.
С научной же точки зрения, исследование природы фотокаталитического эффекта, механизма действия фотокатализаторов чрезвычайно интересно. В 1998 году ежемесячно выходило около 150 публикаций, посвященных фотокатализу. Помимо чисто прикладных работ растет число публикаций, в которых сообщается об исследовании фотокаталитических процессов различными физическими методами. Наиболее плодотворны здесь методы ЭПР (электронного парамагнитного резонанса) и ИК (инфракрасной) спектроскопии, которые позволяют регистрировать промежуточные продукты превращения органических соединений на поверхности ТiО2 и в ряде случаев идентифицировать захваченные электрон и дырку.
Однако до сих пор невозможно ответить на вопрос, почему близкие по свойствам (близкий размер частиц, одинаковая кристаллическая модификация) образцы ТiО2 могут сильно различаться по фотокаталитической активности. Например, белая краска на кузове автомобиля состоит из диоксида титана, но гидрофильными или каталитическими свойствами не обладает.
Фактически фотокатализ дает уникальную возможность глубоко окислять органические соединения в мягких условиях. А простота самих устройств позволяет надеяться на прекрасные перспективы использования фотокатализа на практике. В настоящее время к широкому выпуску фотокаталитических очистителей воздуха приступили такие известные фирмы как Toshiba, Sharp, ТОТО.
Еще одно применение ТiО2-покрытия связано с устранением запотевания стекла или зеркал.
Запотевание стекла связано с плохой смачиваемостью поверхности, то есть образованием на поверхности слоя мелких капелек воды, рассеивающих свет. Поверхность стекла или зеркала чаще всего плохо смачивается из-за загрязнения органическими веществами, которые попадают на них из воздуха или при касании, например, руками. Тонкая прозрачная пленка фотоактивного ТiO2 под действием света разрушает органические загрязнители, поверхность хорошо смачивается, и вода, попадающая на такую поверхность, не собирается в капельки, а растекается по поверхности, а затем испаряется без появления пятен и полос. Глазом наличие такой пленки обнаружить невозможно. Интересно наблюдать, как с одной половины зеркала с ТiО2-покрытием запотевание исчезает в течение нескольких секунд, а на второй половине долго сохраняется, если подышать на это охлажденное зеркало. Выпуск таких зеркал будет освоен в ближайшем будущем.
Из вышесказанного следует, что использование покрытий, содержащих диоксид титана (TiO2) позволяет одновременно дезинфицировать и очищать воздух и воду практически от всех вредных примесей. Фотокатализ не требует применения дорогих окислителей (окислителем является атмосферный кислород - О2), катализатор (TiO2) - безопасное, недорогое, устойчивое соединение. Свет, необходимый для осуществления окисления, может быть натуральным или искусственным. Процесс не требует применения дополнительных и опасных реагентов.
На данный момент существует несколько зарубежных фирм, выпускающих в промышленных масштабах самоочищающиеся стекла и керамическую плитку с TiO2-покрытием – это AFG Industries, Pilkington, PPG Industries, Deutsche Steinzeug Keramik. Компания Pilkington lnc. представляет свое самоочищающееся стекло под торговой маркой - Pilkington Activ™.
Технические характеристики стекла с применением ТiО2-покрытия
|
Код стекла с покрытием |
К пр, % |
К отр, % |
К отр.ст, % |
К уф, % |
Кпр.с.,% |
|
71 |
26 |
26 |
46 |
78 | |
|
68 |
29 |
28 |
45 |
69 | |
|
62 |
27 |
21 |
30 |
31 | |
|
45 |
28 |
15,5 |
22 |
27 |
где,
• К уф % - пропускание в ультрафиолетовом диапазоне спектра;
• К пр % - пропускание в видимом диапазоне спектра;
• К отр % - отражение в видимом диапазоне спектра со стороны покрытия;
• К отр.ст % - отражение в видимом диапазоне спектра со стороны стекла;
• К пр.с. % - пропускание солнечной энергии в видимом и инфракрасном диапазоне излучения.
Фото объектов с применением самоочищающегося стекла
В ЧЕМ ВОЛШЕБНАЯ СИЛА TiO2 ПОКРЫТИЯ?
Диоксид титана – один из самых распространенных материалов в нашей повседневной жизни. Он широко используется в красках, косметике и пищевых продуктах. Сегодня ежегодное потребление диоксида титана в мире превышает три миллиона тонн. Специалисты считают, что потребление диоксида титана тесно связано с жизненным уровнем в стране.
Диоксид титана, который используется как пигмент в краске, отличается от диоксида титана, который используется как фотокатализатор.
Диоксид титана является полупроводником и становится химически активным только после его облучения ультрафиолетовым светом. Длительное время химическая активность диоксида титана под воздействием ультрафиолетового света была проблемой, которую необходимо было решить, когда TiO2 использовался как белый пигмент в краске, так как краска могла менять свой цвет.
 С другой стороны, диоксид титана как фотокатализатор позволяет этой активности играть положительную роль, а именно, разлагать такие материалы, как грязь, сажа, химические препараты и раздражители, токсические препараты, запах дыма сигарет, бактерии или органические материалы. По этой причине можно ожидать, что разработка фотокаталитических технологий на основе TiO2 скоро станет новой отраслью промышленности уже в этом столетии.
С другой стороны, диоксид титана как фотокатализатор позволяет этой активности играть положительную роль, а именно, разлагать такие материалы, как грязь, сажа, химические препараты и раздражители, токсические препараты, запах дыма сигарет, бактерии или органические материалы. По этой причине можно ожидать, что разработка фотокаталитических технологий на основе TiO2 скоро станет новой отраслью промышленности уже в этом столетии.Научное изучение фотокатализа на TiO2-покрытиях началось около 30 лет назад. За это время направление научных исследований менялось несколько раз. Первоначально, фотокаталитическую способность диоксида титана пытались применить для получения водорода из воды, затем пристальное внимание привлекла способность TiO2-покрытия уничтожать вирусы и раковые клетки, разлагать органические загрязнения. В настоящее время уже более 1000 фирм, используя уникальные свойства TiO2-покрытия, создают технологии и оборудование для очистки воздуха и воды.
Например, это покрытие может защитить стекла, используемые на осветительных приборах в туннелях, от загрязнения выхлопными газами автомобильного транспорта. Грязь и сажа не задерживается на брезенте, который покрывает крышу Tokyo Dome (Токио). Здания Оперы в Сиднее (Sydney Opera House) не очищалось бы дождевой водой, если бы на крыше не было TiO2-покрытия. Используя ту же технологию, можно уберечь ветровые стекла, зеркала и очки от «запотевания» водяным паром. TiO2, как фотокатализатор, проявляют изумительные бактерицидные и дезинфицирующие свойства.
Приведенные выше примеры использования диоксида титана показывают, насколько различны функции фотокатализаторов на основе TiO2. Новшества в развитии технологии фотокатализа могут изменить восприятие людей, как о чистоте, так и об очистке окружающей среды.
Что может послужить тому причиной?
Современные методы очистки базируются на предотвращении неконтролируемого попадания отходов, прежде всего, в воздух, воду и почву.
Общепринятыми методами очистки и дезинфекции является хлорирование и озонирование, использование бактерицидных ламп, применение различных фильтров, использование высоких температур или дезинфицирующих веществ. Все эти методы имеют избирательное действие, т.е. они не в состоянии обезвредить все группы микроорганизмов или устранить химические загрязнения. И, последнее, после того как «вредные» вещества уже «пойманы» различными фильтрами необходимо решить, а куда же деть отловленную гадость.
Именно по этой причине пристальное внимание специалистов, работающих в области охраны окружающей среды, сосредоточено на поиске процессов и методов, позволяющих преобразовывать вредные вещества в безопасные компоненты, а заодно и уничтожить патологические микроорганизмы.
 Использование фотокаталитического окисления или гетерогенного фотокатализа позволяет решать обе упомянутые задачи одновременно.
Использование фотокаталитического окисления или гетерогенного фотокатализа позволяет решать обе упомянутые задачи одновременно. Гетерогенный фотокатализ – безопасный и высокоэффективный способ разложения веществ и микроорганизмов до абсолютно безвредных компонентов под действием света в присутствии катализатора. В качестве катализатора используются широко известные полупроводники на основе оксидов металлов (TiO2, ZnO, Fe2O3 и др.).
В большинстве случаев в качестве катализатора используется TiO2, как наиболее устойчивое, недорогое и безопасное, химически и биологически инертное соединение, обладающее наибольшей фотокаталитической активностью при освещении натуральным или искусственным светом.
Первыми процесс фотокаталитического расщепления воды для получения водорода на TiO2 электродах описали Fujishima и Honda в 1972.
В 1985 году Matsunaga с сотрудниками впервые сообщили о бактерицидной активности TiO2. С этого времени исследования в этом направлении получило широкое распространение во всем мире.
За последние годы тысячи химических соединений, большинство из которых занесены в список основных загрязняющих веществ и токсинов, вирусов и раковых клеток были тестированы на возможность их окисления в процессе гетерогенного катализа. Лучше всего изучены: углеводороды и их производные, спирты, эфиры, фенолы, альдегиды, кислоты.
 Основную роль в процессе расщепления веществ на поверхности фотокатализатора под действием света играет образование свободных носителей заряда – электронов и дырок при облучении поверхности фотокатализатора (TiO2) светом с длиной волны менее 390 нм.
Основную роль в процессе расщепления веществ на поверхности фотокатализатора под действием света играет образование свободных носителей заряда – электронов и дырок при облучении поверхности фотокатализатора (TiO2) светом с длиной волны менее 390 нм.Процессы разложения происходят при комнатной температуре и не требуют применения опасных и дорогостоящих препаратов, а в качестве источника света могут быть использованы стандартные лампы дневного света либо натуральный солнечный свет.
Фотокаталитическое разрушение вещества применяют в случаях, когда традиционные средства очистки не помогают, в частности, при уничтожении пестицидов, отходов военных предприятий (тяжелые металлы, авиационное топливо, органические вещества, обезжиривающие агенты и другие химические побочные продукты от производства оружия) или химических красителей. Положительные результаты были достигнуты при очистке воды от экстрагенов (половые гормоны, использующиеся при производстве многих медикаментов), которые вызывают серьезные нарушения в развитии живых организмов или рост раковых заболеваний у людей.
Исследования показали, что чувствительность микроорганизмов к фотокаталитическому расщеплению уменьшается в следующем порядке:
• вирусы;
• бактерии;
• споры бактерий.
За последние годы фотокаталитические пленки TiO2 становятся все более и более привлекательными для использования в различных областях, в первую очередь, при создании дополнительных или основных фильтров для дезинфекции и очистки воды и воздуха.
Помимо бактерицидного действия TiO2 обладает также способностью к самоочищению.
В последнее время особое внимание уделяется созданию самоочищающихся и обладающих противотуманным эффектом поверхностей с покрытием из TiO2.
НА ЧЕМ ОСНОВАНЫ СВОЙСТВА ПОКРЫТИЯ К САМООЧИЩЕНИЮ?
Поверхность любых материалов обычно отталкивает воду. Степень отталкивания воды веществом можно выразить с помощью контактного угла капли воды к поверхности. На стекле или других неорганических материалах, вода имеет контактный угол, колеблющийся от 30 до 90 градусов. У пластика контактный угол обычно от 70 до 80 градусов. У водоотталкивающего пластика угол может превышать 80 градусов.
В настоящее время неизвестны вещества, на поверхности которых угол наклона капли воды был менее 10 градусов. И только пленка из диоксида титана может похвастаться такими результатами.
Тонкая пленка, состоящая из TiO2 фотокатализатора, в сочетании с подходящими добавками демонстрирует начальный контактный угол для воды от 30 до 80 градусов. На этой же поверхности, когда ее подвергают ультрафиолетовому облучению, капля воды меняет контактный угол. Угол постепенно уменьшается и после 4…24 часов облучения достигает почти нуля градусов. На этом этапе, поверхность из гидрофобной (боящейся воды) становится полностью гидрофильной (любящей воду) и такую поверхность называют “супергидрофильной”.
Поверхность сохраняет небольшой контактный угол для воды в течение 1-2 дней без дополнительного облучения ультрафиолетовыми лучами. Затем контактный угол медленно увеличивается, и поверхность становится снова гидрофобной. Но, «супергидрофильность» легко восстанавливается при последующем воздействии на поверхность ультрафиолетовым светом. Короче говоря, TiO2-покрытие является единственно известным практическим «супергидрофильным» материалом, который демонстрирует свои стабильные свойства.
ПРИНЦИП ДЕЙСТВИЯ ТiО2 КАК ФОТОКАТАЛИЗАТОРА
ТiО2 – полупроводниковое соединение. Согласно современным представлениям, в таких соединениях электроны могут находиться в двух состояниях – свободном и связанном. В первом состоянии электроны движутся по кристаллической решетке, образованной катионами Тi4+ и анионами кислорода O2-. Во втором состоянии – основном, электроны связаны с каким-либо ионом кристаллической решетки и участвуют в образовании химической связи. Для перевода электрона из связанного состояния в свободное состояние, необходимо затратить энергию не менее 3,2 эВ. Эта энергия может быть доставлена квантами света с длиной волны < 390 нм (ультрафиолетовое излучение). Таким образом, при поглощении света в объеме частицы ТiО2 рождаются свободный электрон и электронная вакансия (в физике полупроводников такая электронная вакансия называется дыркой).
Электрон и дырка – достаточно подвижные образования и, двигаясь в частице полупроводника, часть из них рекомбинирует (возвращается в связанное состояние), а часть выходит на поверхность и захватывается ею.
Захваченные на поверхности электрон и дырка, являются вполне конкретными химическими частицами. Химически они чрезвычайно активны.
 В терминах окислительно-восстановительных потенциалов реакционная способность электрона и дырки на поверхности ТiО2 характеризуется следующими величинами: потенциал электрона -0,1 В, потенциал дырки ~ +3 В относительно нормального водородного электрода. Иными словами, электрон способен реагировать с кислородом, рождая мощные окислительные радикалы O- и ОН.
В терминах окислительно-восстановительных потенциалов реакционная способность электрона и дырки на поверхности ТiО2 характеризуется следующими величинами: потенциал электрона -0,1 В, потенциал дырки ~ +3 В относительно нормального водородного электрода. Иными словами, электрон способен реагировать с кислородом, рождая мощные окислительные радикалы O- и ОН.Дырка реагирует либо с водой, либо с любым адсорбированным органическим (в ряде случаев и неорганическим) соединением.
ОН- или О- радикалы также способны окислить любое органическое соединение. И таким образом, поверхность ТiО2 под светом становится сильнейшим окислителем.
Последовательность реакций в пленке ТiО2 проходит несколько стадий:
• поглощение света – рождение электрон - дырочных пар;
• диффузия электронов и дырок к поверхности полупроводника;
• объемная рекомбинация электронов и дырок;
• поверхностная рекомбинация электронов и дырок;
• полезные реакции электронов и дырок с адсорбированными молекулами.
К сожалению, к настоящему моменту нет надежных объяснений, связывающих активность ТiО2-покрытия с его свойствами. Из практики известно, что наибольшей фотокаталитической активностью обладают образцы ТiО2 с кристаллической модификацией анатаза и не содержащие большого числа примесей. Поэтому изготовление активного ТiО2-покрытия – предмет опыта каждой компании. Тем не менее, практически все, кто занимается прикладным фотокатализом, обладают оригинальными методиками синтеза высокоактивного ТiО2.
С научной же точки зрения, исследование природы фотокаталитического эффекта, механизма действия фотокатализаторов чрезвычайно интересно. В 1998 году ежемесячно выходило около 150 публикаций, посвященных фотокатализу. Помимо чисто прикладных работ растет число публикаций, в которых сообщается об исследовании фотокаталитических процессов различными физическими методами. Наиболее плодотворны здесь методы ЭПР (электронного парамагнитного резонанса) и ИК (инфракрасной) спектроскопии, которые позволяют регистрировать промежуточные продукты превращения органических соединений на поверхности ТiО2 и в ряде случаев идентифицировать захваченные электрон и дырку.
Однако до сих пор невозможно ответить на вопрос, почему близкие по свойствам (близкий размер частиц, одинаковая кристаллическая модификация) образцы ТiО2 могут сильно различаться по фотокаталитической активности. Например, белая краска на кузове автомобиля состоит из диоксида титана, но гидрофильными или каталитическими свойствами не обладает.
Фактически фотокатализ дает уникальную возможность глубоко окислять органические соединения в мягких условиях. А простота самих устройств позволяет надеяться на прекрасные перспективы использования фотокатализа на практике. В настоящее время к широкому выпуску фотокаталитических очистителей воздуха приступили такие известные фирмы как Toshiba, Sharp, ТОТО.
Еще одно применение ТiО2-покрытия связано с устранением запотевания стекла или зеркал.
Запотевание стекла связано с плохой смачиваемостью поверхности, то есть образованием на поверхности слоя мелких капелек воды, рассеивающих свет. Поверхность стекла или зеркала чаще всего плохо смачивается из-за загрязнения органическими веществами, которые попадают на них из воздуха или при касании, например, руками. Тонкая прозрачная пленка фотоактивного ТiO2 под действием света разрушает органические загрязнители, поверхность хорошо смачивается, и вода, попадающая на такую поверхность, не собирается в капельки, а растекается по поверхности, а затем испаряется без появления пятен и полос. Глазом наличие такой пленки обнаружить невозможно. Интересно наблюдать, как с одной половины зеркала с ТiО2-покрытием запотевание исчезает в течение нескольких секунд, а на второй половине долго сохраняется, если подышать на это охлажденное зеркало. Выпуск таких зеркал будет освоен в ближайшем будущем.
Из вышесказанного следует, что использование покрытий, содержащих диоксид титана (TiO2) позволяет одновременно дезинфицировать и очищать воздух и воду практически от всех вредных примесей. Фотокатализ не требует применения дорогих окислителей (окислителем является атмосферный кислород - О2), катализатор (TiO2) - безопасное, недорогое, устойчивое соединение. Свет, необходимый для осуществления окисления, может быть натуральным или искусственным. Процесс не требует применения дополнительных и опасных реагентов.
На данный момент существует несколько зарубежных фирм, выпускающих в промышленных масштабах самоочищающиеся стекла и керамическую плитку с TiO2-покрытием – это AFG Industries, Pilkington, PPG Industries, Deutsche Steinzeug Keramik. Компания Pilkington lnc. представляет свое самоочищающееся стекло под торговой маркой - Pilkington Activ™.
Статьи в тему: